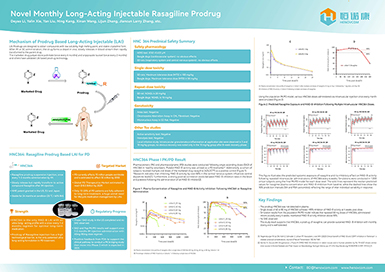
【转发动脉网报道】自研“mRNA加帽核苷酸原料”,恒诺康医药突破mRNA上游原料瓶颈
新冠疫情的爆发带火了mRNA疫苗赛道,2021年至2022年新冠mRNA疫苗的收入已超过500亿美元,上游市场近100亿美元。长期来看,除了新冠疫苗,mRNA技术在肿瘤疫苗、基因编辑、CAR T细胞治疗、蛋白替代疗法及其他传染病预防性疫苗领域都已经逐步成熟,陆续有产品落地。得益于mRNA疫苗、mRNA药物开发周期短、生产工艺容易放大等优势,mRNA已成为近年来生物医药领域的研发热点。
下游市场爆发往往推动上游市场需求,mRNA领域的爆发却凸显出中国上游储备技术的不成熟,因为目前国产mRNA产品的核心加帽元件仍旧依赖进口。无论是mRNA疫苗还是mRNA药物,其关键原材料都是核苷酸,而其中具有高技术壁垒的核心元件“加帽核苷酸原料”和“修饰核苷酸”在原材料成本中占比超过40%~50%。
目前,全球拥有高端加帽原料(Clean Cap)化合物知识产权的公司只有美国Trilink公司一家,国内mRNA企业如果想要基于新一代加帽技术进行相关产品开发,上游原料供应则只能依赖进口。高端加帽原料的制备工艺复杂,每克价格高达100万元,高昂的成本给国内mRNA疫苗和药物企业设置了巨大的研发壁垒,成为了制约我国mRNA疫苗和药物相关领域发展的“卡脖子”技术。
为了实现mRNA行业自上而下的全产业链替代,使中国mRNA产业发展自主可控,恒诺康医药自主开发国产替代的共转录加帽原料产品,团队成员凭借自身在核苷酸领域30余年的积累,以及数月的潜心开发,公司优化了三磷酸合成工艺,并最终在2022年开发了系列mRNA疫苗和药物核苷三磷酸原料,涉及NTPs、PseudoUTP(假尿嘧啶)、N1-Me-pseudoUTP、Modified NTPs、ARCA、以及专利第三代共转录加帽原料LZCap。
恒诺康医药即广州市恒诺康医药科技有限公司,成立于2013年,是一家临床阶段的新药研发公司,公司开发的创新药物包括新型抗病毒、抗纤维化、抗肿瘤以及中枢神经系统药物等,旗下进展最快的管线1类抗流感创新药已在美国完成Ⅰ期临床试验,治疗非特发性肺纤维化的1类新药在美国完成Ⅰa期临床试验,治疗帕金森的2.1类长效药物也已经申报IND。目前,公司在新药专利方面已经获得15项相关发明专利授权。
值得一提的是,在疫情爆发后,恒诺康医药新设了“抗疫”相关管线,其中为了满足下游mRNA相关产品的开发,公司还自主搭建了核苷三磷酸合成与服务平台,以最具竞争力的质量和价格为全球生物制药、疫苗、诊断以及细胞与基因治疗公司提供优质的高端核苷酸产品及服务,包括mRNA疫苗及药物原料 (LZCap、PseudoUTP、 NTPs、ARCA)、分子诊断试剂原料(荧光标记核苷三磷酸、生物素标记核苷三磷酸、dNTPs)、核酸测序原料(荧光标记核苷三磷酸、dNTPs)等产品。
恒诺康基于平台技术,优化了假尿苷三磷酸(N1-Me-PseudoUTP)的合成工艺,N1-Me-PseudoUTP可用于代替常规的UTP,可以减少生成mRNA免疫原性,提高mRNA的表达;在mRNA体外转录的过程中使用N1-Me-PseudoUTP,在进入体内时,可以避免先天免疫传感器的识别,从而阻止TLR3、TLR7、TLR8、RIG-I和其他先天免疫传感器的激活,从而减少IFN1、IL-6和TNF-α的产生,降低免疫刺激,提高mRNA疫苗和药物的安全性。BioNTech 与Moderna已上市的新冠疫苗都使用了修饰核苷酸假尿嘧啶。恒诺康还自主开发了全新结构的加帽原料LZCap,能够提升mRNA加帽率高达95%以上,提高mRNA的稳定性并显著提高蛋白表达量。
01 什么是“共转录加帽”?恒诺康医药助力mRNA开发工艺简化、成本降低
转录是DNA生成RNA的过程。在这个过程中,会先以DNA为模板生成未成熟的premature RNA,再经过细胞核内一系列的后转录修饰,形成成熟的mRNA。mRNA是后续翻译氨基酸形成蛋白质的模板。
成熟mRNA包含5个结构:5' 帽子结构(5' cap)、5' 非翻译区(5' UTR)、编码抗原的开放阅读框、3' 非翻译区(3' UTR)和一个PolyA尾。其中,帽子结构对mRNA来说至关重要。帽子结构不仅可以调节mRNA的剪切成熟,帮助RNA转录产物穿过核膜的选择性孔道,而且还能保护mRNA不被核酸外切酶降解,与翻译起始因子蛋白协同工作,招募核糖体,并协助核糖体与mRNA结合,使翻译开始。
所以,在开发mRNA产品时,体外修饰过程变得十分关键,mRNA疫苗或者药物需要形成帽子结构,才能在体内稳定表达。不过传统的体外修饰mRNA方法主要基于酶加帽法,以dsDNA作为模板,经过转录形成未加帽的mRNA,再经酶促反应成为mature的带帽mRNA。
不过这种方法的弊端在于,使用牛痘病毒的加帽酶价格昂贵,酶促成本高。另外,由于酶加帽引入了额外的蛋白,导致制备工艺复杂,需多次纯化,增加了QA/QC检测项。而新一代的“共转录加帽”则是利用帽类似物直接进行体外转录生成带帽结构的mRNA,实现了“一锅法”mRNA制备,工艺流程简便,也可迅速提升mRNA疫苗和药物的产能。
据悉,BioNTech上市的新冠疫苗BNT162b2正是采用了共转录加帽工艺。但是该工艺由于涉及高昂的专利费,国产厂商急需一款能够避开专利壁垒去实现“共转录加帽”的国产替代方法。恒诺康医药则成为了肩负起这个“重担”的人,公司基于核苷修饰经验和核苷三磷酸产业化工艺,研究开发了新一代核苷酸加帽原料。
恒诺康医药创始人张健存介绍,公司开发的核苷酸酸加帽原料“LZCap”对标海外CleanCap,可以满足“一锅法”mRNA制备,达到比Clean Cap更高的mRNA产率和蛋白表达量。LZCap是一种帽状三聚体,通过化学合成的方式生成带cap1结构的帽子,体外共转录加入LZCap可以产生天然的Cap1结构的mRNA,将mRNA加帽效率提高到了95%以上,为传统加帽方法低效率(ARCA)或酶成本高的问题提供了新的解决方案。
目前公司正在扩建2200㎡专业GMP设施、生产体系和分析质量体系,以确保多公斤级Batch产能。
02 双轮驱动,自主研发抗病毒及神经系统疾病新药,4条管线完成IND
除了“共转录加帽”产品,恒诺康医药在发展的近十年时间里,还建立了包含小分子药物设计和合成、综合分析质量以及制剂研究、药代和nonGLP安全评估、原料药工艺和GMP-like工艺开发及生产的四大技术平台,并有多个项目进入临床和临床前研究阶段:
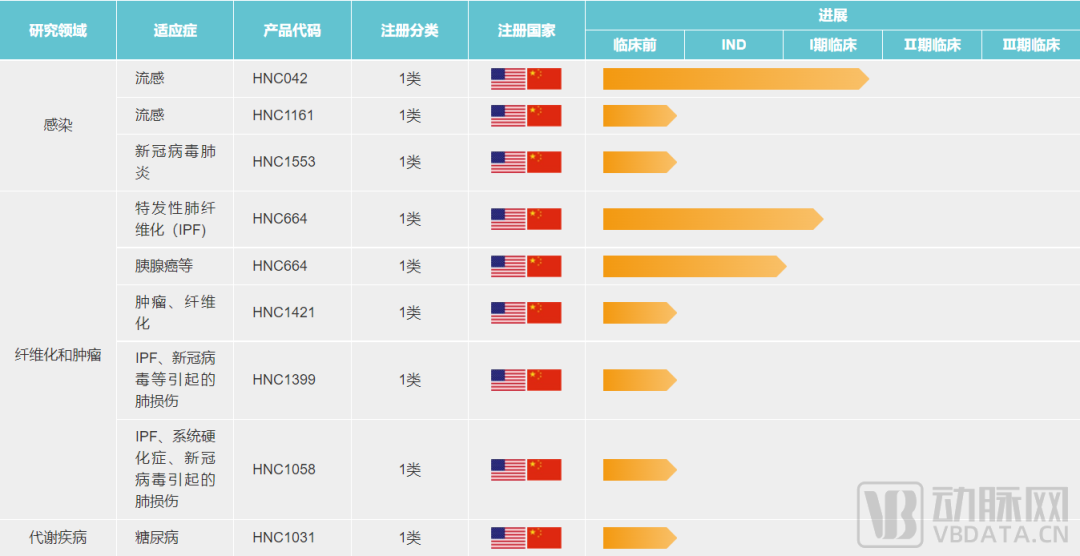
▲ 恒诺康医药临床管线进度
从创新药自主研发,到攻克技术壁垒自主生产国产“共转录加帽”产品,恒诺康医药紧跟市场需求变化,“两条腿”走路、双轮驱动企业发展,不仅提供mRNA上游技术原料,还布局丰富的创新药管线,为人类健康提供更好的解决方案。
据悉,恒诺康医药即将完成pre-B轮融资,募集资金将加速公司旗下创新药管线的推进,以及核酸原料基地的建设等。